
一、什么是表面活性劑?
無論是任何種類的表面活性劑,其分子結構都由性質不同的兩部分組成,一部分是由疏水親油的非極性基團(通常是碳氫鏈組成的,但也可能包括硅氧烷基團、氟碳鏈或其他非極性基團),另一部分為親水疏油的極性基團,常見的極性基團包括羧酸鹽(-COO?)、磺酸鹽(-SO??)、磷酸鹽(-PO?2?)、銨鹽(-N?R?)和羥基(-OH)等。這兩部分的結合使得表面活性劑能夠在水和油等不相溶的介質之間起到界面活性作用,降低表面張力,從而實現乳化、分散、潤濕等多種功能。

圖1:十二烷基苯磺酸鈉的化學結構式(一種常見的陰離子表面活性劑),其分子結構由兩部分組成:一個長鏈的非極性疏水部分--十二烷基(CH3-(CH2)10-CH2-)和一個極性的親水部分--(苯磺酸鈉基團(-C6H5-SO3Na)
不過并不是所有的兩親分子都是表面活性劑,只有碳氫鏈在8~20碳原子的兩親分子才能稱為表面活性劑。碳氫鏈太短,親油性太差,不具備兩親性,而碳氫鍵太長,親水性太差,也不能作為表面活性劑。
表面活性劑傳統的功能是潤濕、洗滌、乳化、分散、發泡、消泡等,但在納米材料領域中不僅利用了表面活性劑的傳統功能,同時還利用其結構特點開發出表面活性劑的微型反應器功能、偶聯功能、成膜功能、官能團反應功能等。
二、什么是臨界膠束濃度(CMC)
兩親性分子與水發生相互作用時會表現出非常獨特的行為,分子的親水基團(極性部分)尋求與水相互作用,而疏水基團(非極性部分)則避免與水的相互作用。當兩親性分子添加到水中時,它們會在空氣-水界面處定向,親水部分在水中,疏水部分在空氣中(下圖B),另一種存在形式是膠束(下圖C),其疏水部分朝向球形結構的內部,由外層的親水殼層包裹和保護,從而形成穩定的分子聚集體。

圖2 A)兩親性表面活性劑分子 B)表面活性劑分子在空氣-水界面處定向 C)在高濃度下,形成膠束。
表面活性劑存在于液體表面或膠束中的分子比例取決于其添加濃度。在低濃度時,表面活性劑占據液體的表面,當表面擠滿表面活性劑時,額外的分子將形成成膠束。這一濃度被稱為臨界膠束濃度(CMC)--表面張力最小值和表面張力呈線性下降交點的臨界點,可通過測量表面張力計算得到。下圖顯示的是表面張力與添加表面活性劑的對數濃度之間的關系,第1階段,表面活性劑濃度很低時,表面張力只檢測到輕微的變化;第2階段,增加表面活性劑,表面張力降低;第3階段,表面完全鋪滿,表面張力不再改變。

圖3 表面張力與表面活性劑濃度的關系(對數刻度)
圓球形并非是表面活性劑膠束的在溶液中唯一存在形式,下圖是不同濃度下,表面活性劑存在的一些形式。①當表面活性劑在水溶液中濃度較小時,膠束主要呈球狀結構,如下圖(b)所示;②當表面活性劑在油性溶液中濃度較小時則形成反膠束,如下圖(c)所示,親油基朝外,親水基朝里;③當水溶液中表面活性劑的濃度大于臨界膠束濃度10倍以上時,膠束會呈棒狀結構,如下圖(d)所示;④當表面活性劑溶液中表面活性劑的濃度更大時,棒狀結構的膠束會生長成為束很長的柱狀結構膠束,這些長的柱狀膠束會相互聚集成更大的六方柱狀膠束,如下圖(e)所示;⑥當濃度更大時,則會形成層狀膠束,如下圖(f)所示。

圖4 表面活性劑的一些存在形式:a單體,b膠束,c反膠束,d棒狀膠束,e六方相,f層狀相,
臨界膠團濃度是表征表面活性劑結構與性能的一個最重要的物理量,根據表面活性劑CMC值大小可以設計表面活性劑加入量以得到膠束大小、形狀可控的溶液。
二、表面活性劑在溶液法納米粉體的作用
表面活性劑親水親油的結構使其在溶液中具有形成膠束的特性。這些膠束在溶液中成為微型反應器,被廣泛用于納米粉體材料的合成與制備中,尤其是使用溶液法制備納米粉體材料時,幾乎都用表面活性劑作為超微反應試劑。目前納米粉體材料制備采用表面活性劑的方法有:沉淀法,超微乳法,乳化法,溶膠-凝膠法等。表面活性劑在納米粉體制備中主要起到如下作用。
1、表而活性劑膠團形成納米反應器
表面活性劑分子在溶液中除可以形成表面活性劑的溶液、乳液外,還可以在溶液內部自聚,形成多種形式的分子有序組合體,如膠束、反膠束、微乳、液晶和囊泡等。這些分子有序組合體的質點大小或微集分子厚度已接近納米數量級,可以在化學反應中作為微反應器為其提供特殊的微環境。
表面活性劑在溶液中的特點是隨著濃度提高,形成膠團。這些膠團的數目、大小在一定條件下是熱力學穩定的,一般情況下,膠團的尺寸為1~1000nm,隨著表面活性劑濃度加大,膠團數目增多,膠團尺寸逐漸變小,達到一定濃度時,膠團粒徑小于100nm,甚至更小。例如,超微乳、微乳液是熱力學上的穩定體系,液滴尺寸分布窄具有較高的單分散性,液滴直徑在10~100nm,所以,利用控制膠團尺寸、形狀的方法可以得到粒徑在10~100nm范圍內的理想納米粉體材料。
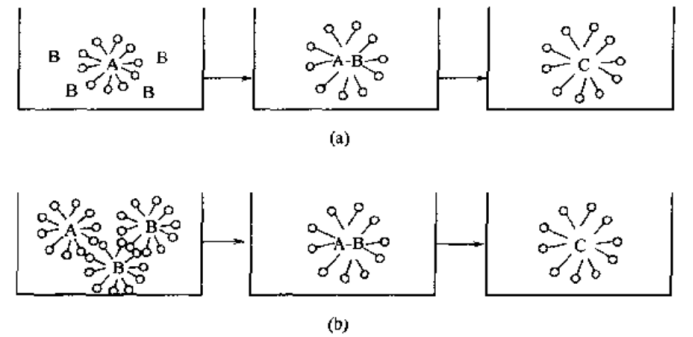
圖5膠團微型反應器模型
在圖中4-1(a)中,反應物B不斷地進入膠團,在膠團內的反應物A和進入的反應物B反應,生成產物C,產物在結構上可能是晶體、無定型物等的沉淀、而反應物從性質上可能是金屬氧化物、非金屬氧化物、純金屬、復合物、高分子化合物等。隨著反應進行,膠團尺寸并不會變大,因為膠團尺寸限定了產物顆粒的大小,因此,所合成微粒尺寸大小是可調可控的。這類反應如沉淀法、共沉淀法、界面法、相轉移法等。
在圖4-1(b)中,反應物A和反應物B分別處于不同的膠團中在A膠團和B膠團接觸時,A或B溶人對方膠團中,進行反應生成產物C,最后,形成含有C的膠團。C膠團的大小一般不會因為AB的結合增大,但是,C膠團的表面同時含有AB膠團的成分,這種反應方法有微乳法、溶膠凝膠法等。
2、空間位阻效應
在納米粉體制備過程中,顆粒容易團聚形成較大的二次顆粒,影響分散性和性能。因此如何防止一次顆粒團聚生成二次顆粒,是納米粉體制備過程中需要重點注意的問題。
在膠團微型反應器中,產物晶核隨反應進行而漸漸長大,表面活性劑在顆粒表面使膠體內吸附層帶負電,此時加入相反電荷助劑可通過庫侖交互作用有效地平衡膠體微粒表面電荷,形成雙電層,抑制團聚的發生,使粉體的團聚體尺寸變小。
在膠體形成階段,表面活性劑吸附在膠體表面,親水基朝外,憎水基朝里,包覆在膠粒的表面形成空間阻擋層,使顆粒之間的團聚不易發生。在干燥過程中,隨著水的脫附,膠粒周圍水溶液中的表面活性劑分子的疏水基朝向氣相,親水基進入水中,形成單分子膜,降低了水與空氣的接觸面,表面張力急劇下降,使膠體的顆粒與顆粒之間不易靠近,從面起到分散的作用,防止了團聚的發生。如下圖。

圖6納米微粒膠團外表雙電層空間位阻效應
3、降低表面能
表面活性劑形成膠團,內部反應終止后,表面活性劑在產物外表包覆,形成低表面能的單分散顆粒,由于表面活性劑的存在,納米顆粒表面張力降低,表而能小,使顆粒之間無法重新團聚形成二次顆粒。并且表面活性劑外露一端的基團,在納米微粒分散和與其他材料復合時,可以起到親和劑的作用。
4、靜電作用
表面活性劑膠團在水溶液中的外表面形成雙電層,雙電層外層電荷將排斥同種電荷,這導致體系中,膠團之間相互排斥,無法靠近,使每一個膠團成為獨立的反應器。表面活性劑的靜電效應也被利用于納米顆粒的表面修飾和粉體的分散中。
參考資料:
1、Biolin Scientific百歐林科技,檢測方法/臨界膠束濃度
2、表面活性劑-原理、合成、測定及應用(第二版),趙世民一編
3、表面活性劑與納米技術,李玲編著
編輯:Alpha

作者:Alpha
總閱讀量:1112